生物脱氮新工艺及其技术原理
王建龙
(清华大学 环境科学与工程系,北京 100084)
摘 要:介绍了生物脱氮领域最近开发的若干新工艺,为水处理工艺设计提供了新的理论和思路。
关键词:生物脱氮;新工艺;技术原理
中图分类号: X703
文献标识码:B
文章编号:1000-4602(2000)02-0025-04
由于常规的活性污泥工艺过程中硝化作用不完全,反硝化作用则几乎不发生,总氮(TKN)的去除率仅在10%~30%之间。因此,对于城市污水、含氮工业废水,若采用常规的活性污泥法处理,出水中还含有大量的氮(NO3-)和磷,引起受纳水体富营养化。这就促使人们对传统的活性污泥工艺流程进行改造,以提高N、P的去除效果,如A/O法、A2/O法等工艺。这些工艺在废水脱氮除磷方面起到了一定的作用,但仍存在以下问题:?
① 硝化菌群增殖速度慢且难以维持较高生物浓度,特别是在低温冬季。因此造成系统总水力停留时间较长,有机负荷较低,增加了基建投资和运行费用;?
② 系统为维持较高生物浓度及获得良好的脱氮效果,必须同时进行污泥回流和硝化液回流,增加了动力消耗及运行费用;
③ 抗冲击能力弱,高浓度氨氮和亚硝酸盐进水会抑制硝化菌生长;?
④ 为中和硝化过程产生的酸度,需要加碱中和,增加了处理费用。
最近的一些研究表明:生物脱氮过程中出现了一些超出人们传统认识的新现象,如硝化过程不仅由自养菌完成,异养菌也可以参与硝化作用[1];某些微生物在好氧条件下也可以进行反硝化作用[2];特别值得一提的是有些研究者在实验室中观察到在厌氧反应器中NH3-N减少的现象[2~5],这些现象的发现为水处理工作者设计处理工艺提供了新的理论和思路。
1 SHARON 工艺
SHARON工艺(Single reactor for High activity Ammonia Removal Over Nitrite)是由荷兰Delft技术大学开发的脱氮新工艺[6]。其基本原理为简捷硝化—反硝化,即将氨氮氧化控制在亚硝化阶段,然后进行反硝化。硝化过程可分为两个阶段,第一步是由亚硝化菌(Nitroso monas)将氨氮转化为亚硝酸盐(NO2-),亚硝化菌包括亚硝酸盐单胞菌属和亚硝酸盐球菌属。第二步是由硝化菌(Nitrobacter)将亚硝酸盐转化为硝酸盐(NO3-),硝化菌包括硝酸盐杆菌属、螺旋菌属和球菌属。这类菌利用无机碳化物如CO32-、HCO3-和CO2作碳源,从NH3、NHO4+或NO2-的氧化反应中获得能量,两步反应均需在有氧条件下进行。生成的NO3-由反硝化菌在缺氧条件下还原成N2或氮氧化物。
亚硝化菌和硝化菌的特征总结如表1。
SHARON工艺具有以下特点:
①硝化与反硝化两个阶段在同一反应器中完成,可以简化工艺流程;
②硝化产生的酸度可部分地由反硝化产生的碱度中和;
③可以缩短水力停留时间(HRT),减小反应器体积和占地面积。
如果将硝化过程控制在亚硝化阶段,实现简捷硝化—反硝化,则该工艺还具有下述优点 :?
① 可节省反硝化过程需要的外加碳源,以甲醇为例,NO2-反硝化比NO3-反硝化可节省碳源40%;?
②可减少供气量25%左右,节省动力消耗。?
然而,将硝化阶段控制在亚硝化阶段的成功报道并不多见.这是因为,硝化菌(Nitrobacter)能够迅速地将亚硝酸盐转化为硝酸盐.SHARON工艺的成功在于:巧妙地应用了硝化菌(Nitrobacter)和亚硝化菌(Nitrosomonas)的不同生长速率,即在较高温度下,硝化菌的生长速率明显低于亚硝化菌的生长速率(见图1)。
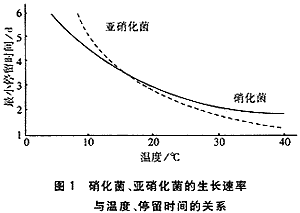
因此,在完全混合反应器中通过控制温度和停留时间,可以将硝化菌从反应器中冲洗出去(wash out),使反应器中亚硝化菌占绝对优势,从而使氨氧化控制在亚硝化阶段。同时通过间歇曝气,可以达到反硝化的目的。
2 ANAMMOX工艺?
1990年,荷兰Delft技术大学Kluyver生物技术实验室开发出ANAMMOX工艺(ANaero bic AMMonium OXidation)[7],即在厌氧条件下,以NO3-为电子受体,将氨转化为N2。最近研究表明,NO2-是一个关键的电子受体。由于该菌是自养菌,因此不需要添加有机物来维持反硝化。实验研究发现:厌氧反应器中NH4+浓度的降低与NO3-的去除存在一定的比例关系。发生的反应可假定为:
5NH4++3NO3-→4N2+9H2O+2H+
ΔG=-297kJ/molNH4+
最近研究表明,NO2-也可作为电子受体进行如下反应:
NH4++NO2-→N2+2H2O
ΔG=-358kJ/molNH4+
根据化学热力学理论,上述反应的ΔG<0,说明反应可自发进行,厌氧NH4+氧化过程 的总反应是一个产生能量的反应。从理论上讲,可以提供能量供微生物生长。因此,可以假定厌氧反应器中存在微生物,它可利用氨作为电子供体还原硝酸盐,或者说它可利用硝酸盐 作为电子受体来氧化氨。
ANAMMOX工艺的可能途径如图2所示[8]。
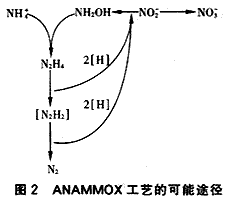
NH4+的厌氧氧化途径及反应自由能变化总结于表2。?
3 De?ammonification工艺 ?
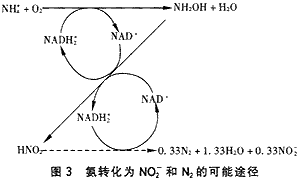
Hippen等人[9]报道了一个适用于处理高浓度含氮废水的新工艺。该工艺中,氨转化为氮气的过程不需要按化学计量式消耗电子供体,这种特殊的转化过程命名为“aerobic de?ammonification”(好氧反氨化)工艺。该工艺中涉及到的微生物目前尚不太清楚。工艺的关键是控制供氧。Muller等人[10]也报道过自养硝化污泥在非常低的氧压力下(1kPa或气相中约2.0%O2)可以产生氮气。当溶解氧压力在0.3kPa时,氨的最大氧化率达58%。然而,该过程还未实现稳定和可行的工艺设计。Binswanger等人[11]报道过利用生物转盘反应器通过硝化—反硝化工艺去除高浓度NH4+废水中的氨。结果表明:当表面负荷为2.5gN/(m2·d)时,去除速率达90~250gN/(m2·d)。在整个过程中,不需要添加任何可生物降解的有机碳化合物。反应机理可假定为:反应过程中生成的NO2-被NAD+还原。如图3所示。
4 OLAND工艺?
该工艺称为Oxygen Limited Autotrophic Nitrification Denitrification(氧限制自养硝化反硝化),简称OLAND工艺,由比利时Gent微生物生态实验室开发。该工艺的关键是控制溶解氧,使硝化过程仅进行到NH4+氧化为NO2-阶段,由于缺乏电子受体,由NH4+氧化产生的NO2-氧化未反应的NH4+形成N2。该反应机理为由亚硝化菌(Nitrosomonas)催化的NO2-的歧化反应。该工艺涉及到的化学反应,反应自由能及其与传统工艺的比较总结如表3所示。
(kJ/molN) △G
(kJ/mol反应) 传统的硝化—反硝化工艺: NH4++2O2→NO3-+H2O+2H+ -349.3 -349.3 NO3-+H++0.83CH3OH→0.5N2+2.17H2O+0.83CO2 -546.1 -546.1 NH4++2O2+0.83CH3OH→0.5N2+3.17H2O+H++0.83CO2 -895.4 -895.4 ILAND工艺: 0.5NH4++0.75O2→0.5NO2-+0.5H2O+H+ -217 -135.5 0.5NH4-+0.5NO2-→0.5N2+H2O -358.8 -179.4 NH4-+0.75O2→0.5N2+1.5H2+1.5H2O+H- -316 -316 与传统工艺比较,OLAND工艺可节省: O2 62.5% 碱度 0% 电子供体 100%
5 结语
上述工艺如ANAMMOX、OLAND等,其基本原理为氨的氧化与NO2-的还原相偶联,从理论上讲并不新颖。早在1972年Ritchie等人就已经从他们的研究中得出结论:认为脱氮中间产物N2O既可以由氨和羟氨在好氧条件下产生,也可以由NO2-在好氧或厌氧条件下还原产生。众多研究表明:硝化过程中氮氧化物的产生随氧浓度的降低而增加。Poth等人从一系列15N同位素示踪实验发现:亚硝化菌(Nitrosomonas europaea)可利用NO2-作为终端电子受体进行反硝化,导致氮氧化物的产生。而上述工艺的新颖之处在于利用这些生化原理开发出了实用可行的生物脱氮新工艺。
参考文献:
[1] Kuenen J G, Robertson L A. Combined nitrification?denit rification process[J].FEMS Microbiol Rev,1994,15(2):109-117.
[2] Munch E V ?et al?.Simultaneous nitrification and denitrificati on in bnech?scale sequencing batch reactors[J]. Wat Res,1996,30:277-284.
[3] Stepanov A L,Korpela T K.Microbial basis for the biotechnologi cal removal of nitrogen oxides from flue gases[J]. Biotechnol Appl Biochem,199 7,25(2):97-104.
[4] Graff A A ?et al?.Anaerobic oxidation of ammonium is a biologic ally mediated process[J]. Appl Environ Microbiol,1995,61:1246-1251.
[5] 王建龙.NH4+的厌氧氧化[J].生命的化学,1997,17(6):3 7-38.
[6] Jetten M S M ?et al?.Towards a more sustainable municipal waste water treatment system[J]. Wat Sci Tech,1997,35(9):171-180.
[7] Straous M et al?. Ammonium removal from concentrated wastestreams with the anaerobic ammonium oxidation(ANAMMOX)process in different configur ations[J]. Wat Res,1997,31:1955-1962.
[8]Graff A A ?et al?.Autotrophic growth of anaerobic ammonium?oxidi zing micro?organisms in a fluidized bed reactor[J]. Microbiolgy,1996,142:2187-2196.
[9] Hippen A ?et al?.Aerobic deammonification:a new experience in the ttreatment of wastewater[J]. Wat Sci Tech,1997,35:111-120.
[10]Muller E B ?et al?.Simultaneous NH3 oxidation and N2 production at reduced O2 tension by sewage sludge subcultured with chemolitrophic medium[J]. Biodegradation,1995,6:339-349.
[11]Bingwanger S et al?. Simultane Nitrifikation/Denitrifikati on vo n stark Ammonium?belasten Abwasser ohne organische Kohlenstoffquellen[J].Korr espondenz Abwasser,1997,44:1573-1580.
电 话:(010)62785684?
传 真:(010)62771472?
E-mail : wangjl@tsinghua.edu.cn?
收稿日期: 1999-09-17
论文搜索
月热点论文
论文投稿
很多时候您的文章总是无缘变成铅字。研究做到关键时,试验有了起色时,是不是想和同行探讨一下,工作中有了心得,您是不是很想与人分享,那么不要只是默默工作了,写下来吧!投稿时,请以附件形式发至 paper@h2o-china.com ,请注明论文投稿。一旦采用,我们会为您增加100枚金币。








